自从耐思开展“SCI论文奖励计划”以来,我们收到了大量申请。如今我们的产品已经被写入了百余篇杰出的实验成果当中!
在此,我们甄选了数篇论文,与广大科研工作者共同研读、积极探讨!
文章标题
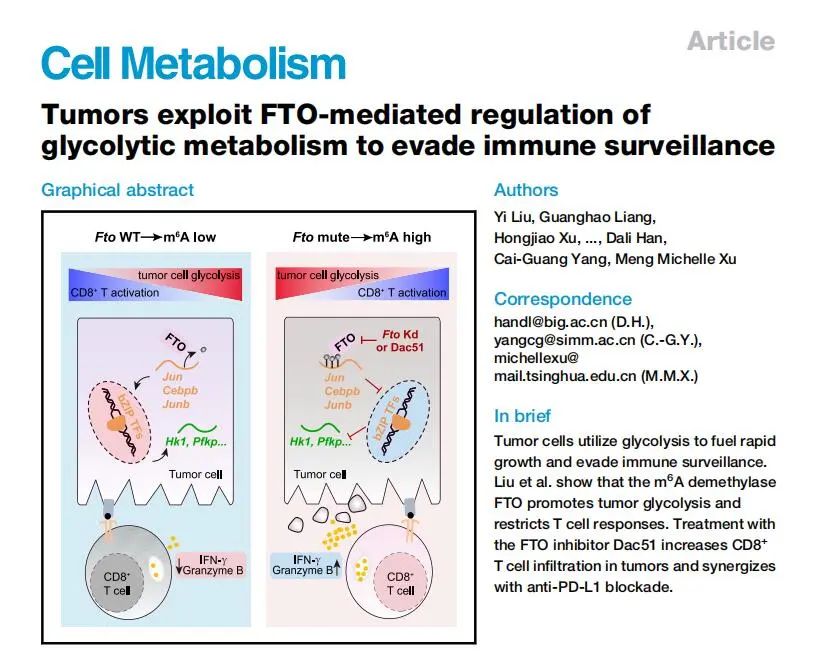
Tumors exploit FTO-mediated regulation of glycolytic metabolism to evade immune surveillance
第一作者:
刘弋 董文鑫 梁广豪 徐洪蛟 董泽
通讯作者:
清华大学徐萌研究员
中国科学院上海药物研究所杨财广研究员
中国科学院北京基因组研究所韩大力研究员
内容总结
CD8+ T细胞是机体识别与杀伤肿瘤细胞的关键免疫细胞,其功能却常常被复杂的肿瘤微环境所抑制。前期研究表明,肿瘤细胞可利用多种表观修饰机制调节T细胞介导的抗肿瘤免疫应答,从而实现免疫逃逸。而m6A作为一种动态可逆的表观转录组修饰,影响mRNA的稳定性及翻译等过程,在肿瘤的发生发展中起到重要的作用。然而,肿瘤细胞的m6A修饰如何参与调节肿瘤免疫微环境,调控T细胞介导的免疫监视,目前仍不太清楚。
研究人员发现,在不同实体瘤细胞中敲低m6A的去甲基化酶FTO,均能抑制肿瘤在小鼠体内的生长,并增加肿瘤中浸润的抗原特异性CD8+ T细胞的比例。进一步的研究表明,在肿瘤中敲低FTO会使CD8+ T细胞更快地激活,更有效地执行杀伤肿瘤细胞的功能。通过对RNA-seq、MeRIP-seq (m6A-seq)、ATAC-seq、ChIP-seq等多维组学测序数据的整合分析发现,FTO可调控多个bZIP家族转录因子的m6A修饰,并促进其mRNA稳定性。这些bZIP家族转录因子能促进糖酵解基因的表达,增强肿瘤细胞糖酵解活性,进而抑制CD8+ T细胞的激活。
基于此,研究者以靶向FTO的小分子抑制剂Dac51为小分子工具,进一步地验证了FTO在实体瘤中通过调控肿瘤糖酵解,逃逸免疫监视的机制。随后,在小鼠模型中分别采用了PD-L1阻断和Dac51小分子的治疗,发现其均能有效抑制肿瘤在小鼠体内生长,而联合PD-L1和Dac51能大幅提升治疗效果。另外,研究者在病人肿瘤样本建立的类器官模型中也发现,Dac51处理能有效地增强T细胞的抗肿瘤免疫应答,提示了Dac51在临床应用上的可能性。综上,研究者提出,m6A去甲基化酶FTO可作为免疫治疗的有效靶点,对RNA修饰进行干预将有望成为免疫治疗的新策略。
耐思助力产品
 |
 |
 |
 |
 |
 |
