LC-MS 实验室超纯水的处理建议和方法
[摘要]:本文用实验案例说明了实验室环境和纯水的储存对纯水质量的影响,对比 LC-MS 级别超纯水以及瓶装水,阐释了在 LC-MS 实验室应用中 Milli-Q 超纯水的优势。
实验室环境和纯水的储存
避免长期储存纯水,并且避免纯水暴露在实验室环境当中。
实验室环境中含有多种污染物(有机物质,碱金属,细菌,塑料等),因此纯水暴露在实验室环境中或者使用纯水过程中有多种转移步骤都会导致水质下降。实践证明,长期储存纯水会增加纯水与实验室环境的接触。这一结果会导致高 MS 背景噪音(图 1),金属加合物的产生和信号的抑制(图 2)。
图1.超纯水储存和暴露在空气中与新鲜制备的纯水的效果对比
上图:某品牌LC-MS级别纯水储存4周,并反复开盖数次。
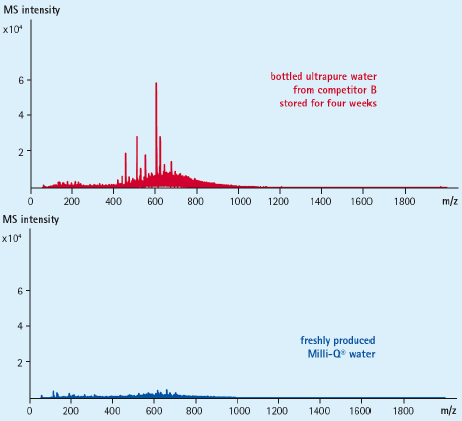
下图:Milli-Q超纯水
检测方法:
MS:Bruker Esquire 3000+离子阱流速:0.2mL/min
温度:25°C
进样方式:MS直接进样
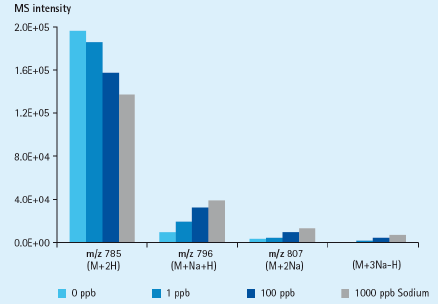
图 2 钠离子的存在增加了加合物的形成并对信号产生抑制作用
分析方法:
样品:500pmol的Glu-Fibrionopeptide溶解于50/50乙*/水(混合了不同浓度的氯化钠) 分析仪器:Waters Synapt HDMS
进样模式:正ESI模式直接质谱进样
技术影响
• MS产生背景噪音
• 质谱图谱变得更复杂
• 形成加合物峰
• 信号抑制
• 灵敏度简单
• 增加LOD
(Ⅱ)存储容器材质
避免塑料储存容器
操作及储存纯水过程中避免使用塑料容器,如塑料瓶或锥形瓶等。塑料容器比较容易引入
一些普遍存在的添加剂(抗静电剂,稳定剂和塑化剂),这些都会导致鬼峰,并提高背景噪音(图 3)。建议使用表面特殊处理的棕色玻璃瓶或硼玻璃。标准玻璃瓶中,硅和碱金属的释放会形成加合物(请参考图 2 中钠离子的影响)。
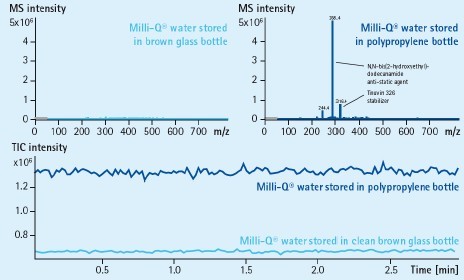
图3. 使用聚丙烯瓶储存超纯水
上图:棕色玻璃瓶和塑料瓶中储存的超纯水MS谱图下图:棕色玻璃瓶和塑料瓶中储存的超纯水TIC谱图
仪器及分析方法:Bruker Esquire 3000+离子阱 ESI+模式,直接进样分析
技术影响
• LC-MS分析中会出现鬼峰,并对信号产生抑制作用
• 灵敏度降低,LOD值增加
• 增加背景噪音
• 质谱变得更加复杂
(Ⅲ)玻璃器皿的清洗
避免使用洗瓶机
洗瓶机操作时需要用大量的洗涤剂,其中含有很强的碱和表面活性剂。碱会使碱金属和硅从玻璃中溶解出来,而硅则会附着在玻璃表面。
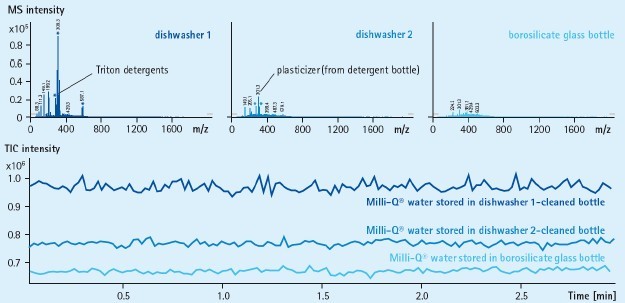
图4. 洗瓶机清洗后的质谱玻璃器皿对质谱的影响:
Milli-Q制备的超纯水分别储存在两种不同品牌洗瓶机和LC-MS级别水/乙*清洗后的玻璃瓶中后的MS谱图及TIC谱图
进样方式:直接进MS样,ESI+模式
技术影响
• LC-MS分析中会出现鬼峰
• 灵敏度降低,LOD值增加
• 增加背景噪音
• 质谱变得更加复杂
• 形成加合物
(Ⅳ)纯水系统的使用
超纯水使用前弃去前段水
滞留在纯水系统中的水会随着时间的推移质量下降。存在在试验室环境中的污染物也会被
中端精制器上的滤膜富集在表面,再收集纯水的过程中会使水质污染。因此,在收集纯水之前建议有冲洗纯水系统的过程,例如,周末过后弃掉开始的几升水,每天在收集纯水前弃掉 250-500mL 水。
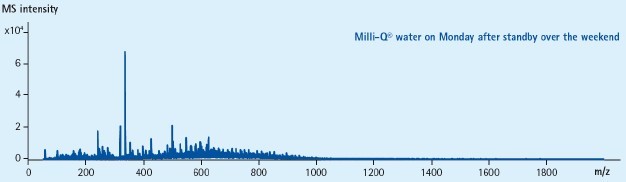
图5A. 长时间未使用(比如,周末),并且没有冲洗流程的超纯水系统收集的超纯水的MS谱图。
上述质谱使用的超纯水是经过周末后从超纯水系统中产出的超纯水

图5B.冲洗流程的超纯水系统收集的超纯水的MS谱图
上述质谱使用的超纯水是超纯水系统使用过一段时间后新鲜制备的
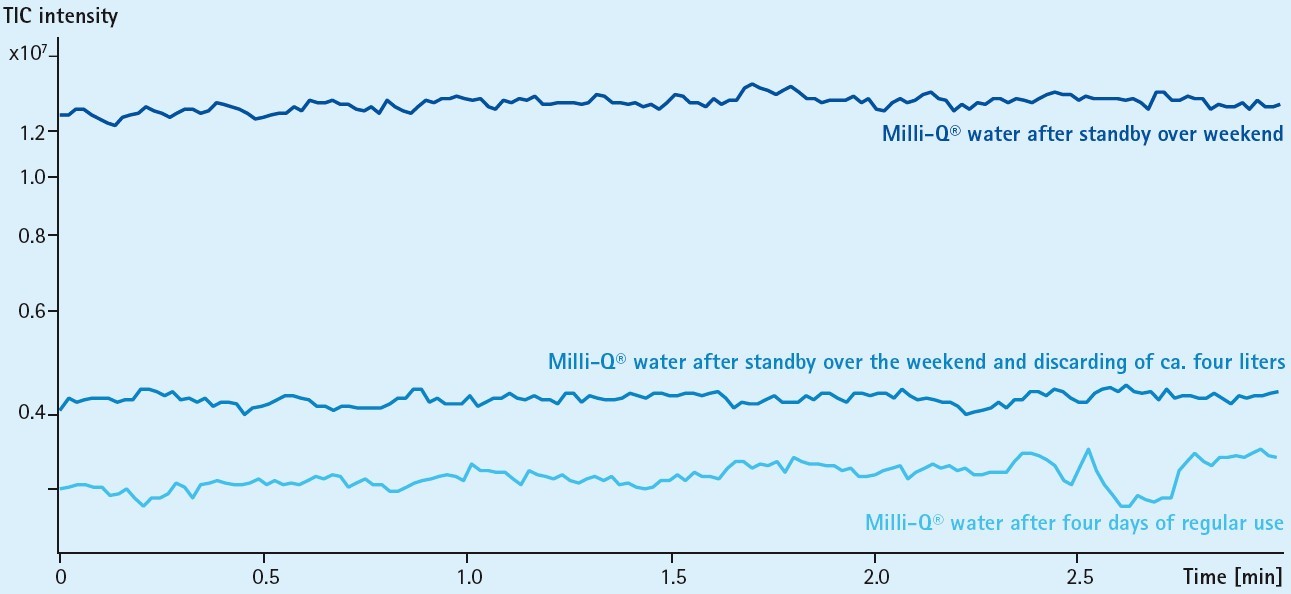
图 5C.对比不同时间点 Milli-Q®超纯水 TIC 谱图对比。上述分析方法:
MS:Bruker Esquire 3000+ ion trap MS system,
进样模式:ESI+, 直接 MS 进样流速:0.2 mL/min
温度:25°C.
技术影响
• MS背景噪音
• MS图谱变得复杂
• 信号抑制
• 灵敏度降低
• LOD 增加
结论:
Milli-Q 超纯水系统正确的安装和维护能够满足 LC-MS 实验用水的需求;新鲜的超纯水比储存的超纯水或暴露在空气中的超纯水能得到更好的实验结果。超纯水应使用玻璃容器承装, 并且玻璃容器不能用洗瓶机洗涤。
