类器官有多热?
类器官并不是这两年的才兴起的研究热点,早在2013年,《Science》杂志就将类器官评为“年度十大技术”,2017年类器官荣获《Science methods》生命领域的“年度技术”,到了2019年,类器官甚至成功登上了《Science》杂志的封面。
作为前沿热点技术之一,类器官不仅获得了诸多学术界顶刊的推荐,还早已获得我国的官方推荐。早在2018年,类器官模型就已经被国自然基金委列为项目指南的推荐技术。2021年国家科技部下发的《关于对“十四五”国家重点研发计划6个重点专项2021年度项目申报指南征求意见的通知》中,也把“基于类器官的恶性肿瘤疾病模型”列为“十四五”国家重点研发计划中首批启动重点专项任务。
近几年类器官在国自然项目申请中的数量也不断攀升,从2021年的46个到2022年的67个。类器官相关研究也必将成为国自然申请中的大热门,中标项目数量可能会继续增长。2023年上半年,“Organoid”相关文章就有2194篇,远超前几年同期水平,意味着该领域的研究热度还在升温。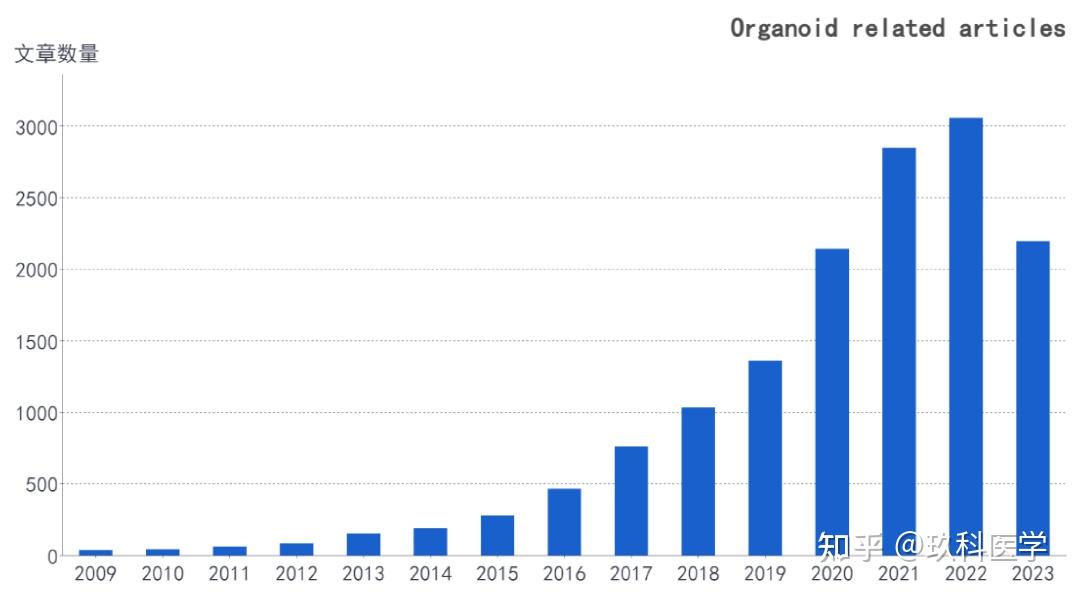
类器官相关文章数量趋势(数据来源:PubMed)
类器官的3D培养系统
类器官(organoid)是体外分化培养的3D细胞培养物,可以通过与对应器官的类似的空间组织重现对应器官的部分功能,从而提供一个高度生理相关系统。
3D细胞培养系统是类器官产生的基础,它通过悬浮培养建立,使用支架或无支架技术以避免细胞与塑料盘的直接物理接触。
➢支架是类似于天然ECM的生物凝胶或合成水凝胶,最常用的Matrigel,是由Engelbreth-Holm-Swarm(EHS)小鼠肉瘤细胞分泌的异质凝胶状蛋白质混合物,它主要包含粘附蛋白,如胶原蛋白、巢蛋白、层粘连蛋白和硫酸肝素蛋白聚糖,类似于细胞外环境,能够为细胞提供结构支持和ECM信号。
➢无支架技术则是细胞在重力和表面张力作用下悬挂在平板上的特定培养基液滴中培养的技术。此外,类器官的3D结构也可以通过“气液界面”建立,在这种情况下,细胞在最初浸没在培养基中的成纤维细胞或基质胶基底层上培养,培养基逐渐蒸发并将上层细胞层暴露在空气中以允许极化和分化。
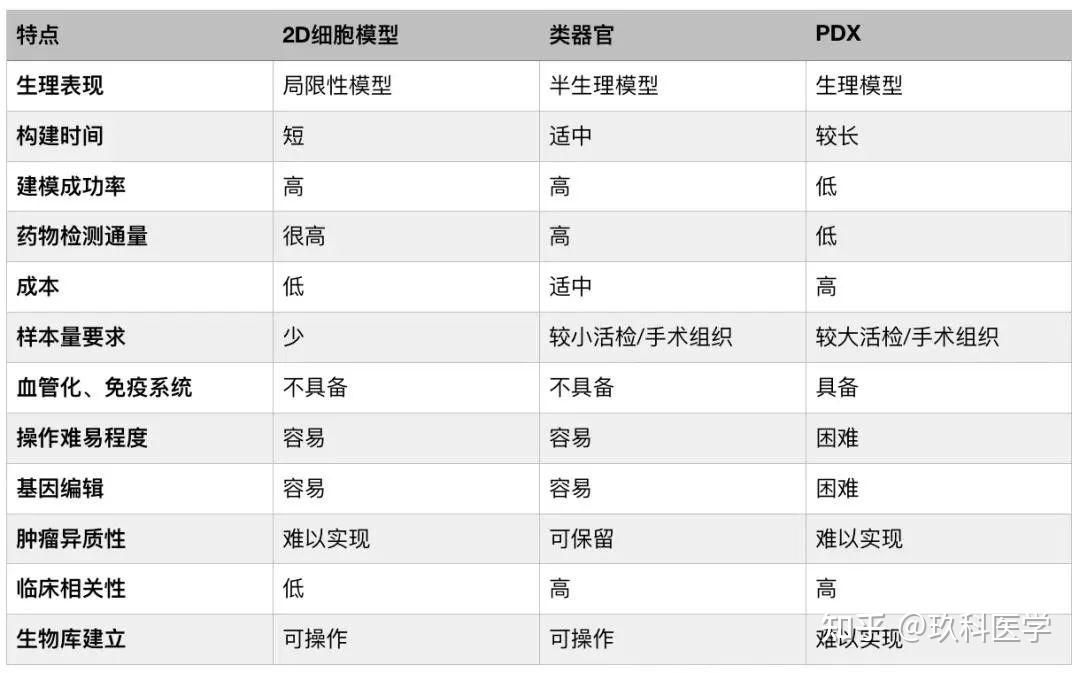
相较于传统2D细胞培养或者昆虫以及哺乳动物等模型,类器官模型在各方面都给予了更大的想象空间。
类器官的培养
类器官可来源于胚胎干细胞(ESC)、诱导多能干细胞(iPSC)、成体干细胞(ASC),或者肿瘤组织。
➢对于ESC/iPSC衍生的类器官,ESC/iPSC在各种细胞生长因子或小分子化合物(抑制剂/激活剂)以及基质胶和细胞培养添加剂的逐步分化方案下,能够按照类似于原肠胚形成和器官发生过程中的发育线索,从三个胚层生成类器官。
➢对于ASC来源的类器官,ASC需要从胎儿或成人组织中产生;获得单个ASC或含有ASC的组织单元之后,再通过3D培养方案形成类器官。
➢对于肿瘤组织来源的类器官,肿瘤组织内含有小部分具有干细胞活性的肿瘤细胞,通过将肿瘤来源的组织细胞或者分离出的肿瘤干细胞等进行3D培养,能够衍生出肿瘤类器官(Tumoroids)。
类器官的应用
类器官作为一个新兴的技术,在科学研究领域潜力巨大,包括发育生物学、疾病病理学、细胞生物学、再生机制、精准医疗以及药物毒性和药效试验。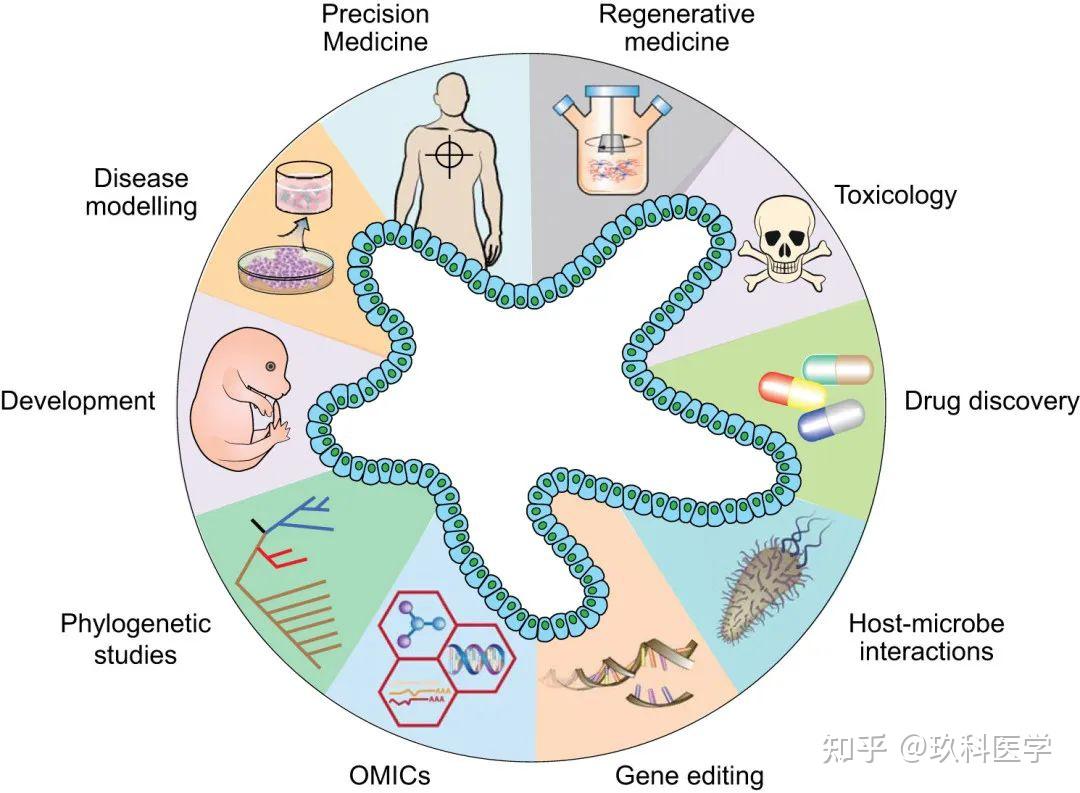
类器官的多种应用方向(PMID: 32459504)
类器官培养使研究人体发育提供了不受伦理限制的平台,为药物筛选提供了新的平台,也是对现有2D培养方法和动物模型系统的高信息量的互补 。此外,类器官为获取更接近自然人体发育细胞用于细胞治疗成为可能。通过类器官繁殖的干细胞群取代受损或者患病的组织,类器官提供自体和同种异体细胞疗法的可行性,未来这一技术在再生医学领域也拥有巨大的潜力。使用这项技术,采用CRISPR/Cas9能够纠正体外遗传异常并能够将健康的转基因细胞再次回输入患者体内,并在后期整合入组织内。
在精准医学应用中,患者衍生的类器官也被证明为有价值的诊断工具。在进行治疗之前,采用从患者样本来源的类器官筛查患者体外药物反应,旨在为癌症和囊胞性纤维症患者的护理提供指导并预测治疗结果。随着类器官培养系统以及其实验开发技术的不断发展,类器官应用到了各大研究领域。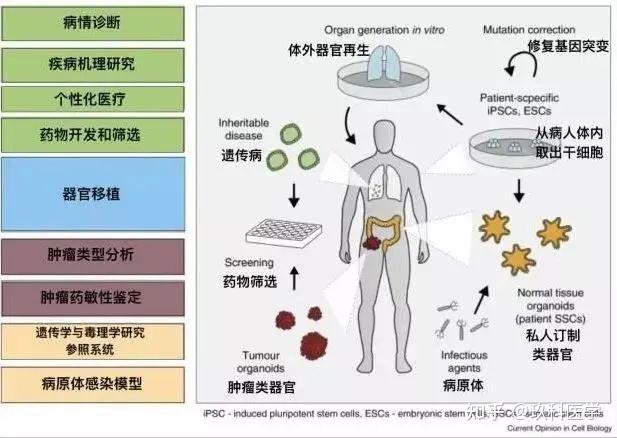
1、通过类器官对发育和疾病进行建模
研究人员可以通过类器官来模拟人类发育和疾病,因为类器官是从人类干细胞或成年细胞产生的诱导性多能干细胞生长而来的,它们的成分和结构也与原发组织相似,并且易于操作和冷冻保存。这意味着类器官可以用于研究源自干细胞的人体组织且难以通过动物模型模拟的人类疾病分析,研究人员仅需少量的起始物质即可培养类器官。
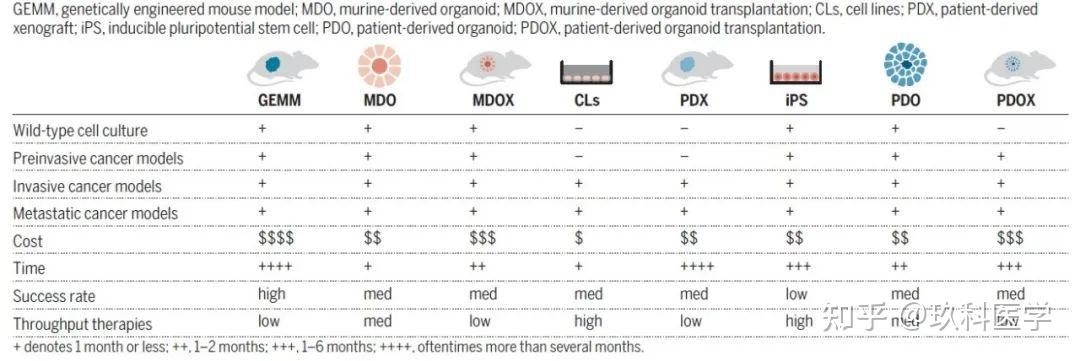
因其与对应的器官拥有类似的空间组织、保持一些关键特性并能够重现部分生理功能,而被认为是检测人类生物学和疾病方面的新模型。相较于细胞系(cell lines)、基因工程鼠(genetically engineered mouse models, GEMMs)和人源化异种移植鼠(patient-derived xenografts, PDX)这些传统的研究模型,类器官模型(鼠源类器官mouse-derived organoids, MDO和人源类器官patient-derived organoids, PDO)不但能够取自正常组织和组织癌变过程中各个阶段的肿瘤组织,而且其培养体系简单易操作,时间和金钱成本较低,且具有较高效率,因而得到广大研究人员的亲赖,被Nature Methods评为2017年生命科学领域年度技术。
2、干细胞类器官工程
干细胞生物工程技术的进步提高了控制细胞类型,组织和相互作用的能力,而类器官工程正需要通过直接修饰干细胞或控制微环境来操纵每个结构层。现在,科学家已经开发了更精确的合成环境,通过用信号蛋白修饰基质的生物惰性区域,可以更好地控制干细胞的活性。类器官工程技术对于一些体内环境成分复杂、需要精确建模的发育研究特别有用。
3、类器官与精准医疗
类器官技术正在成为个体化治疗的工具,运用类器官技术进行个体化治疗是指,通过体外对类器官进行药物筛选和基因型分析,制定适合这个个体的治疗药物和方法。
截至到目前,不同肿瘤PDOs对传统和正在研发的药物所产生的反应是各种各样的。对目前有限的资源研究发现,大部分PDOs所展现的治疗反应和相对应的病人刚开始对治疗的反应是一致的。PDOs也可以用于针对被动或获得性耐受开发新的药物。更重要的是,PDOs对具有细胞毒性的药物敏感性较强,因而可以更好的预测病人使用后的临床反应。接下来,研究人员对大量个体PDOs的药物反应数据进行整合分析,找出共同特征,进而对一类相似病人进行生物标记物开发研究。
➢3.1药物筛选
类器官培养物可用于药物筛选,这可将肿瘤的遗传背景与药物反应相关联。来自同一患者健康组织的类器官的建立提供了通过筛选选择性杀死肿瘤细胞而又不损害健康细胞的化合物来开发毒性较小的药物的机会。自我更新的肝细胞类器官培养物可用于测试潜在新药的肝毒性(临床试验中药物失败的原因之一)。
3.1.1 类器官药物筛选的优势
速度快:类器官构建成功率高以及培养速度快。常规来说,在类器官培养一周之后就可以进行药筛。从样本采集到出具药敏结果的全流程已经可以很好地控制在2周之内。
通量高:从可筛查的药物通量来说,利用类器官不仅可以在孔板上进行多种药物的筛查,每个药物还可以测试不同的浓度,多个实验平行开展。
临床相关性强:类器官用于癌症药筛的临床相关性和预测有效性在多篇研究中都已经得到了较为充分的证实。Vlachogiannis G团队在Science发表了肿瘤类器官体外药敏测试指导临床用药的里程碑式研究,在71位转移性胃肠道癌提取了110份组织构建了类器官,共测试了55种抗癌药物。研究结果显示,类器官药筛达到了93%的特异性,100%的灵敏度、88%的阳性预测率和100%的阴性预测率,展现了极高的临床相关性。
3.1.2 类器官进行药筛的流程
药物筛选流程包括类器官的构建、评估、药敏检测三大方面:
类器官构建:类器官的样本来源通常为肿瘤组织或者胸腹水等恶性积液,主流的培养方法包括较为常用的正置胶滴法、适用于肿瘤和睾丸类器官培养的倒置胶滴法、适用于有气体接触的黏膜类器官(肠、呼吸道)培养的气液界面法以及需要较大扩增(脑类器官)的生物反应器法等。首先将患者来源的肿瘤样本组织通过机械剪切得到肿瘤细胞团,再将细胞团酶消化成单细胞。分离消化后,将细胞嵌入到基质胶中并在96/384孔板上进行胶滴的种接,再覆盖以培养基和细胞因子培养。类器官培养至直径几百微米的细胞小球即可用于药筛。类器官培养特有的重要试剂包括消化液、培养基(例如Wnt、R-Spondin、Noggin等细胞因子)、基质胶(Matrigel等)。
评估:在培养好类器官之后,对于类器官的评估和验证也至关重要。通过基因测序、免疫荧光、HE染色等方法,从形态学、组织病理学以及分子遗传学等多个维度对类器官进行鉴定。评估的目的是确定类器官和原肿瘤具有一致性,这也是进行后续药筛的前提。
药物检测:类器官目前可筛选的药物种类包括化疗药、小分子靶向药、抗体药物等。药筛的核心检测检测指标通常为IC50以及细胞抑制率,根据这些指标在筛查的药物中选取对肿瘤抑制效果最佳的药物。在中国的注册临床中,类器官以化疗药的敏感性检测作为主流应用,类器官用于检测靶向药和免疫治疗的敏感性在未来还有极大的发挥空间和应用潜力。
3.1.3 类器官药筛的发展方向
类器官药筛与二代测序作为组合产品使用,二者在临床上可以有机结合,很好地相辅相成。二代测序从基因层面上检测出患者的靶点突变情况和潜在的药物敏感靶点,为医生和患者提供初步用药选择,但是单凭二代测序结果无法保证完全的临床疗效。部分研究报道和临床案例指出,二代测序筛出的潜在靶向药并没有在实际临床上反应出有效性,这一部分的不确定性通过类器官可以很好排查。
➢3.2 基因型分析
来自不同健康器官的类器官的生长,然后对培养物进行全基因组测序,可以分析器官特异性突变谱。通过生长来自同一肿瘤不同区域的类器官,可以用于研究肿瘤内异质性。区域特异性突变谱可以通过类器官的全基因组测序来揭示。使用与上述相似的方法,可以利用类器官来研究特定化合物对健康细胞和肿瘤细胞突变谱的影响。
类器官的挑战
类器官培养技术目前正处于技术爆发和科研成果井喷的阶段,行业发展具有很大的前景,但也面临较大的挑战。比如如何利用好人体胚胎的干细胞建立持久稳定的体外模型;培养条件和环境刺激如何更真实的模拟还原人体微环境;科研属性的产品如何实现量产,如何转化为临床产品等。
类器官作为新型的药筛模型,成本虽然较PDX更低,但还是远高于细胞系。类器官成本占比较高的包括培养使用的基质胶,常用的基质胶为美国BD Biosciences公司的Matrigel®,在行业内处于较为垄断的地位,价格较高。Matrigel可以产生类似于哺乳动物细胞基底膜的生物活性基质材料,帮助多种类型的细胞达到附着和分化。Matrigel的来源是小鼠肉瘤细胞系,除了成本较高的问题,同时批次间存在一定的变异性。且由于是动物来源,对于有机类的药物的检测有局限性。考虑到小鼠来源的细胞外基质对于药物筛选实验结果存在一定的干扰,因此基质的工程技术开发用于合成外源差异较小的、非动物来源的基质胶用于成本下降和性能优化将是类器官产业化需要解决的关键性问题之一。基质胶以外,培养也涉及多种细胞因子组合使用,细胞生长因子通常也价格不菲。选择效果更好的细胞因子以及尝试减少使用细胞因子的数量也可以带来成本下降的空间。
目前大多类器官本身并不具备血管化的结构。因此,随着类器官体积的增长,类器官受限于氧气的缺失以及代谢废物的增加,可能导致的组织坏死。已有研究构建血管内皮细胞微环境的肿瘤类器官,将类器官肿瘤细胞和血管内皮细胞在Matrigel上共同培养,生成血管结构以期解决类器官血管化缺失的问题。
血管化以外的难点还包括模拟肿瘤和免疫环境的相互作用关系。2019年Nature Protocol发表了肿瘤类器官和免疫细胞共同培养的相关protocol,可以体现和模拟出肿瘤微环境的部分特征。以上皮类器官和免疫细胞共培养模型为例,可通过在培养基中添加活化的免疫细胞、在组织消化成单细胞后和免疫细胞共同生长、添加ECM中的重组细胞因子等方法重塑类器官和免疫细胞的相互作用。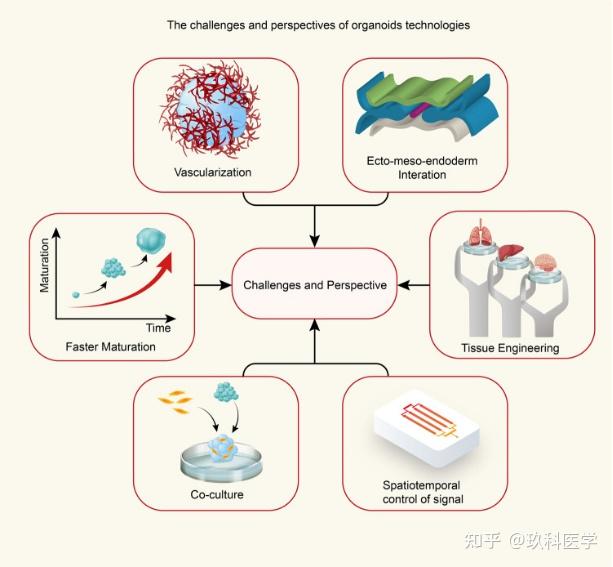
相比于单个类器官,类器官系统的构建能够对药物疗效和潜在毒性做出更完整全面的评估。目前类器官仅能检测出药物对于肿瘤的抑制效果,对于其他器官组织是否存在其他副作用和安全性风险并不能做出预判。为了解决这一问题,2017年Skardal et al.构建了有心脏、肺部、肝脏组成的集成于闭合循环关注体中的类器官系统,以达到全面揭示药物对不同器官的毒性和药效的目的。
重复性(reproducibility)和一致性(consistency)也是类器官发展的重大瓶颈,这很大程度上由于过程控制的欠缺与行业标准的空白。类器官培养过程中人为因素的过多参与、自动化程度低导致因为系统偶然性造成的误差较大。同时,类器官检测手段十分匮乏,活体观察主要集中在形态学观察,断点观察集中在基于荧光的各类指标的检测,能够活体实时对类器官各项指标进行检测的光学、电化学等手段仍较为欠缺。当前,类器官很多研究者致力于制造更新的类器官,做出之前未能做出的类器官,我们可以制作海马体、垂体、腺体、脾、肾的类器官,却难以确定一个符合要求的类器官需要满足那些个体的诸如尺寸、形状、基因表达量等,群体的诸如类器官之间的方差等统计学指标。这将限制类器官的高效研究与向临床研究的转化。
对于类器官培养过程中的工程控制也是亟待解决的问题。当前类器官培养大多使用Matrigel水凝胶作为培养基质,Matrigel是康宁生命科学公司生产的Engelbreth-Holm-Swarm (EHS)小鼠肉瘤细胞分泌的胶状蛋白混合物。Matrigel因其含有外源成分,难以应用在人的很多治疗场景。另一方面,虽然类器官与微流控技术已有一些结合研究的例子,但使用微流控芯片对类器官生存的流体环境进行模拟仍不成熟,如何使用微流控等技术对类器官培养时流体微环境进行控制是亟待解决的问题。同时,现有类器官的直径约在100-500μm之间,虽然具有一定程度的尺度效应,但还是难以模拟真实组织、器官的场景。倘若要制造尺度更大的类器官,类器官的血管化也是十分重要的问题。
总体而言,新兴的类器官技术已经对生物医学研究、个体化医学中的药物筛选以及与基因组编辑技术相结合的基因治疗有用。类器官的广泛应用尚处于探索的初期阶段。广泛的研究将使3D类器官系统能够补充现有的模型系统,这将在未来加强基础和临床研究。
